233 : Diabète sucré de type 1 et 2 de l’enfant et de l’adulte. Complications : Différence entre versions
De Wiki ECN
| Ligne 329 : | Ligne 329 : | ||
=== Traitement médicamenteux === | === Traitement médicamenteux === | ||
*Associé aux règles hygiénodiététiques | *Associé aux règles hygiénodiététiques | ||
| + | ==== Antidiabétiques oraux ==== | ||
{| class="wikitable" | {| class="wikitable" | ||
! !! colspan="2" | Insulinosensibilisateurs !! colspan="5" | Insulinosécréteurs | ! !! colspan="2" | Insulinosensibilisateurs !! colspan="5" | Insulinosécréteurs | ||
| Ligne 349 : | Ligne 350 : | ||
| -1% d'HbA1c, protection cardiovasculaire || -1% d'HbA1c || -1% d'HbA1c || -1% d'HbA1c || -0,5 à 1% d'HbA1c || -0,5 à 1% d'HbA1c || -1 à 1,5% d'HbA1c || | | -1% d'HbA1c, protection cardiovasculaire || -1% d'HbA1c || -1% d'HbA1c || -1% d'HbA1c || -0,5 à 1% d'HbA1c || -0,5 à 1% d'HbA1c || -1 à 1,5% d'HbA1c || | ||
|} | |} | ||
| + | ==== Insulinothérapie ==== | ||
| + | *'''Insulinothérapie combinée''' : | ||
| + | **Association aux hypoglycémiants oraux | ||
| + | **En l'absence de contre-indication aux hypoglycémiants oraux si l'insulinorequérance est partielle | ||
| + | **Commencer par une injection d'insuline intermédiaire type NPH au coucher ou d'analogues lents | ||
| + | **Adaptation progressive des doses d'insuline à la glycémie capillaire à jeun | ||
| + | **Intérêts : dose d'insuline facile à adapter sur la glycémie du matin, moindre prise de poids par rapport à 2 prises d'insuline | ||
| + | *'''Insulinothérapie exclusive''' : | ||
| + | **2 à 4 injections | ||
| + | **Schéma basal/bolus ou mélange rapide/intermédiaire | ||
| + | **'''ASG pluriquotidienne nécessaire''' | ||
| + | **Contre-indique le renouvellement du permis poids lourds ! | ||
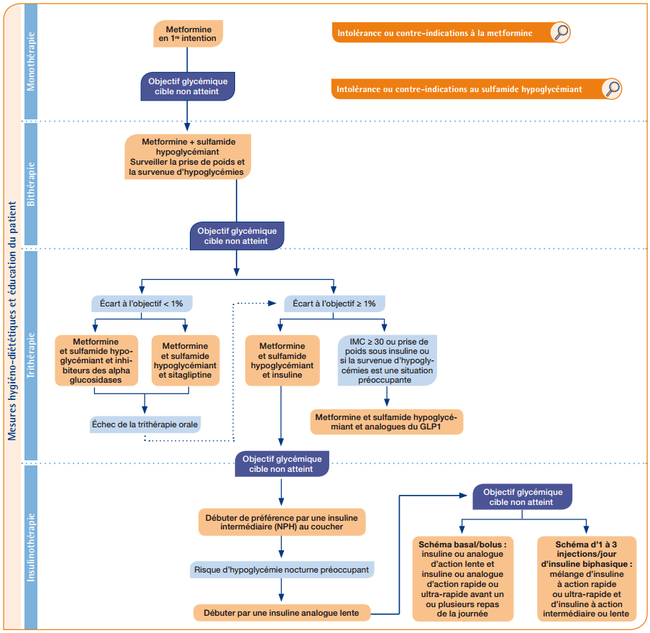
| + | === Stratégie thérapeutique<ref name="Recos HAS 2013 DT2">[http://www.has-sante.fr/portail/upload/docs/application/pdf/2013-02/reco2clics__diabete_type_2.pdf Recommandations HAS 2013 : Diabète de type 2]</ref> === | ||
| + | [[Fichier:StrategieTherapDT2.png|650px|sans_cadre]] | ||
| + | [[Média:StrategieTherapDT2CIMetf.png|Stratégie en cas de contre-indication à la metformine]] | ||
| + | |||
| + | [[Média:StrategieTherapDT2CISulf.png|Stratégie en cas d'allergie aux sulfamides]] | ||
| + | |||
| + | = Complications = | ||
Version du 15 octobre 2013 à 15:37
Sommaire
Objectifs
- Diagnostiquer un diabète chez l’enfant et chez l’adulte
- Identifier les situations d’urgence et planifier leur prise en charge
- Argumenter l’attitude thérapeutique et planifier le suivi du patient
- Décrire les principes de la prise en charge au long cours
Définitions
- Glycémie :
- Normale à jeun < 1,10 g/L
- Hyperglycémie modérée à jeun : 1,10 - 1,26 g/L
- Diabète sucré :
- Glycémie à jeun ≥ 1,26 g/L à 2 reprises
- Ou glycémie aléatoire ≥ 2 g/L et signes cliniques d'hyperglycémie
| Caractéristiques | Type I | Type 2 |
|---|---|---|
| ATCD familiaux du même type | Rares | Fréquents |
| Age de survenue | < 35 ans | > 35 ans |
| Début | Rapide, explosif | Lent, insidieux |
| Facteur déclenchant | Souvent présent | |
| Symptomatologie | Bruyante | Pauvre/absente |
| Poids | Normal ou maigre | Obésité abdominale |
| Hyperglycémie au diagnostic | > 3 g/L | < 2 g/L |
| Cétose | Fréquente | Rare |
| Complications au moment du diagnostic | Absentes | 50% des cas |
| Cause de mortalité | Insuffisance rénale | Maladies cardiovasculaires |
Diabète de type 1
- Prévalence : 200 000 en France, gradient Nord/Sud
- Survient avant 35 ans (adolescence +++)
- Augmentation régulière de l'incidence
- Sex-ratio = 1
Physiopathologie
- Carence absolue en insuline due à la destruction des cellules β-pancréatiques
- 2 sous-types :
- Diabète type 1 auto-immun (90%) : diabète type 1 classique + LADA (Latent Autoimmune Diabetes in Adult)
- Diabète type 1 idiopathique (absence d'auto-anticorps) : diabètes cétosiques du sujet noir, diabètes suraigus japonais
Prédisposition génétique
- Toujours présente, mais pas d'ATCD familiaux dans 85% des cas
- Principaux gènes concernés : Ag de classe 2 type HLA (existe également HLA protecteurs)
- Nombreux gènes impliqués : éléments variables du gène de l'insuline, gène e la protéine CTLA-4, gène PTP-N22
Facteurs environnementaux
- Facteurs génétiques ne suffisent pas à expliquer l'étiopathogénie (50% d'atteinte commune chez les jumeaux homozygotes)
- Nombreux virus suspectés (coxsackie, CMV, rubéole, oreillons)
- Différence importante avec les facteurs précipitant le diagnostic : grippe, stress...
- Théorie hygiéniste
Processus auto-immun
- Principaux antigènes :
- Insuline et pro-insuline
- GAD (Glutamic Acid Decarboxylase)
- IA2 (islet antigen 2)
- Insulite auto-immune avec destruction des cellules β par les lymphocytes cytotoxiques
- Anticorps détectables au diagnostic :
- ICA : anticorps anti-îlots
- Anti-GAD
- Anti-IA2
- Anti-insuline
- Fréquence des autres pathologies auto-immunes associées → polyendocrinopathies auto-immunes type 1 et 2
Diagnostic
Présentation clinique initiale
- Début rapide ou explosif
- Syndrome cardinal : polyuro-polydipsie, amaigrissement, polyphagie
- Troubles visuels transitoires : jours qui suivent le début de l'insulinothérapie +++
- Fonte musculaire (quadriceps), rarement hépatomégalie
- Dyspnée de Kusmall = acidose
- Glycémie veineuse très élevée
- Glycosurie + cétonurie
- Révélation par une acidocétose inaugurale
Formes cliniques
- LADA ou diabète type 1 lent :
- Début tardif et progressif proche du type 2
- Anticorps positifs (anti-GAD +++)
- Insulinothérapie nécessaire en 2 à 10 ans
- Diabète cétosique de l'Africain :
- Début par décompensation cétosique suivie d'une possibilité d'arrêt de l'insuline dans 50% des cas après la phase aiguë
- Possibilité de répétition des épisodes de cétose avec rémission
- Anticorps négatifs
- Diagnostic tardif au stade de coma acidocétosique
- Lune de miel : période suivant le diagnostic du diabète type 1 : équilibre avec doses faibles d'insuline, parfois arrêt
Confirmation diagnostique
- Diagnostic clinique : maigreur + cétose + âge < 35 ans
- Paramètres immunologiques (si triade incomplète) : auto-anticorps ± typage HLA
- Si marqueurs immunologiques négatifs → éliminer d'autres formes de diabète proches du DT1 :
- Diabètes génétiques monogéniques : MODY, mutation du gène de l'insuline, diabètes mitochondriaux, syndrome de Wolfram (diabète insipide, diabète sucré, atrophie optique, surdité)
- Diabètes secondaires : pancréatite chronique, pancréatectomie totale, cancer du pancréas, hémochromatose, mucoviscide
- Diabète néonatal : apparition aiguë dans les 6 premiers mois, peut persister ou régresser et récidiver ; rechercher une origine non-autoimmune
- Autres causes rares :
- Inhibition fonctionnelle de l'insulinosécrétion : hypokaliémie, jeûne prolongé, phéochromocytome, somatostatinome
- Glucagonome
- Insulinorésistance primitive profonde
- Insulinorésistance secondaire : hypercorticisme, acromégalie, hyperthyroïdie
- Diabètes iatrogènes : corticoïdes, immunosuppresseurs, diurétiques hypokaliémiants, progestatifs de synthèse, salbutamol, antiprotéases du SIDA, pentamidine
Evolution
Histoire naturelle
- Modèle d'Eisenbach :
- Phase préclinique : destruction des cellules β par les processus immuns
- Diagnostic clinique : destruction > 85%
- Phase clinique séquellaire : disparition lente des cellules restantes
- Etapes :
- Prédisposition génétique
- Insulite silencieuse
- Diabète préclinique : signes métaboliques précoces, hyperglycémie
- Diabète patent peptide C + : insulinodépendance
- Diabète peptide C - : destruction totale des cellules β
Maladie chronique
- Importante de l'acceptation de la maladie par le patient
- Education : engagement permanent nécessaire du patient pour gérer le traitement et participer aux soins quotidiens
- Freins à l'adhésion :
- Peur des hypoglycémies
- Peur de prendre du poids
- Non-acceptation de la maladie
- Refus des contraintes (adolescent +++)
- Insulinothérapie inadaptée au mode de vie
- Erreurs techniques : injections trop profondes/superficielles, lipodystrophie
- Maladie surajoutée (infection +++)
- Diabète instable :
- Episodes itératifs de céto-acidoses ou hypoglycémies sévères
- Facteurs psychologiques au premier plan
Prise en charge
Principes
- Importance de l'éducation thérapeutique :
- Transfert des connaissances par enseignement collectif ou individuel
- Vérification des comportements et des acquis
- Importance des consultations infirmières et diététiques
- Définir des objectifs thérapeutiques personnalisés et acceptés :
- Réduction du risque cardiovasculaire
- Objectifs idéaux chez le diabétique type 1 non-âgé :
- Glycémie le matin à jeun : 1-1,20 g/L
- Glycémie préprandiale : 0,8-1,2
- Glycémie post-prandiale (2h) : 1,2-1,8
- Au coucher : 1,2
- A 3h du matin : > 0,8
- HbA1c ≤ 7%
- Hypoglycémies : modérées < 5/semaine, pas d'hypoglycémie sévère
- Autocontrôles : 3 à 6 par jour
- 3 à 5 injections/j
- Equilibre délicat de l'insulinothérapie :
- Diminution des complications (rétinopathie, néphropathie, neuropathie, coronaropathie) avec ↓ HbA1c
- Risque d'hypoglycémie sévère si insulinothérapie intensive
- Chez l'enfant jeune et la personne âgée : objectif d'HbA1c plus laxiste
Autosurveillance
- Buts :
- Suivre le diabète
- Adapter les doses
- Avoir une idée de l'équilibre moyen
- Gérer les situations d'urgence
- ASG ≥ 4 ×/j : pré-prandial + coucher, de temps en temps post-prandial et à 3h du matin
- Carnet d'autosurveillance
Surveillance
- Hémoglobine glyquée :
- HbA1c par méthode standardisée
- Normale : 4-6%
- Objectifs : ≤ 7%, 8% chez l'enfant et la personne âgée fragile, 8,5% avant 6 ans
- Reflet de l'équilibre glycémique sur 3 mois : glycémie moyenne (g/L) = 1,5 + (HbA1c - 7)×0,3
- Causes d'erreur de mesure : anémie hémolytique, urémie, hémoglobinopathie, traitement par EPO, saignées → fructosamine
- Bilan métabolique annuel : EAL, créatinine, microalbuminurie, ECBU, ECG
- Dépistage FO annuel
- Consultation spécialisée tous les 3 à 4 mois
Insulinothérapie
- Traitement principal, palliatif, à vie
- Variétés :
- Insuline recombinante : identique à l'insuline humaine
- Insulines rapides : Actrapid, Insuman
- Insulines ralenties : NPH, Ultraltard
- Analogues de l'insuline : structure modifiée à but thérapeutique
- Analogues rapides (juste avant le repas) : Humalogue, Novorapid
- Analogues lents (1 à 2 fois par jour à heure fixe) : Lantus, Levemir
- Parfois mélanges préconditionnés
- Insuline recombinante : identique à l'insuline humaine
- Résorption cutanée dépend de la profondeur, de la zone, de la dose, de l'environnement thermique et de l'activité musculaire du membre concerné
- 2 modes d'administration :
- Stylos à insuline (réutilisables ou UU)
- Pompes portables pour administration continue modulée : plus efficaces mais plus contraignantes et chères
- Schémas :
- Choix selon acceptation, autonomisation, objectifs thérapeutiques
- Schéma basal-bolus : analogues lents couvrant le nycthémère + analogues rapides avant les repas
- 4 injections : 3 rapides pré-prandiales, 1 lente pour couvrir la nuit
- 3 injections : regroupement injection lente et rapide du soir
- Doses en général < 1 UI/kg, à adapter en fonction des glycémies, de l'activité physique et de l'alimentation prévues
- Education thérapeutique pour l'auto-gestion +++ (insulinothérapie fonctionnelle)
- Effets secondaires :
- Hypoglycémies
- Prise de poids : +5 kg en moyenne
- Allergie (rare)
- Lipoatrophie d'origine immunologique
- Lipohypertrophie si piqûre au même endroit
Traitement non-insulinique
- Maladie chronique → suivi multidisciplinaire, consultation d'annonce, soutien et accompagnement
- Alimentation variée sans interdit mais horaires et apports glucidiques réguliers
- Exercice physique
- Associations de patients
Cas particuliers
Diabète de l'enfant et de l'adolescent
- Fréquence des acido-cétoses
- Attention aux hypoglycémies sévères, surtout chez le jeune enfant
- Diabète difficile à équilibrer : ↑ des besoins en insuline, acceptation difficile
- Part croissante de diabète de type 2 chez les enfants obèses
Diabète chez la femme
- Diabète gestationnel
- Contraception : contre-indication aux estroprogestatifs et des progestatifs dérivés des norstéroïdes
- Grossesse :
- Pronostic normal si équilibre périconceptionnel parfait et jusqu'à l'accouchement
- Utiliser des analogues de l'insuline ayant l'AMM chez la femme enceinte
- Retentissement de la grossesse sur le diabète :
- Baisse physiologique de l'HbA1c
- ↑ des besoins en fin de grossesse, ↓ en post-partum
- Risque d'aggravation de la rétinopathie et de la néphropathie si non-stabilisées
- Contre-indication absolue : insuffisance coronaire
- Objectifs glycémiques strictes, suivi rapproché spécialisé mensuel
- Ménopause : éviter l'hormonothérapie substitutive percutanée
Personne âgée
- Ne pas craindre l'insulinothérapie
- Objectifs plus laxistes chez les personnes fragiles à haut risque hypoglycémique
Diabète et jeûne
- Ne jamais arrêter l'insuline en cas d'intolérance alimentaire, essayer des collations liquides fractionnées ou administration de glucose IV
- Vérifier la cétonurie et la cétonémie : troubles digestifs peuvent révéler une cétose
- Hospitalisation systématique en cas de nécessité de jeûne > 1h avec perfusion glucosée et adaptation des doses d'insuline
- Jeûne prolongé nécessaire : insuline IVSE + glucosé IV
Diabète de type 2
- 85% des diabètes, prévalence ~4%
- Prévalence augmente avec l'âge
- Prévalence augmente de 5%/an
- Personnes à risque : obèses, anomalies du métabolisme glucidique, ATCD familiaux de DT2, ethnies (noirs, hispaniques)
- Découvert en général à l'âge adulte
- Insulinorésistance initialement répondant aux antidiabétiques oraux (ADO), insulinorequérance secondaire
Physiopathologie
- Elément central = diminution de la sensibilité à l'insuline, favorisée par l'obésité androïde, l'âge et la sédentarité
- Insulinorésistance :
- Incapacité de l'insuline d'atteindre une réponse maximale au niveau des organes cibles
- Défaut de captation musculaire du glucose
- Accroissement de production de glucose au niveau hépatique → hyperglycémie à jeun
- Insulinopénie relative : insuffisance de sécrétion d'insuline par rapport au niveau de la glycémie
- Facteurs génétiques : si les 2 parents sont diabétiques, 30 à 60% de chance pour le sujet de le devenir
- Glucotoxicité : hyperglycémie aggrave le déficit d'insulinosécrétion et l'insulinorésistance par élévation du seuil du glucose sensor
- Lipotoxicité : insulinopénie → non-freination de la lipolyse → ↑ acides gras libres → diminue l'insulinosécrétion
- Syndrome métabolique lié +++ à l'insulinorésistance :
- Obésité abdominale (PA > 102 (H)/88 (F) cm)
- Hypertriglycéridémie
- ↓ HDL
- HTA
- Hyperglycémie modérée à jeun, →voire diabète
Diagnostic
Clinique
- En général, évolution asymptomatique ou à bas bruit
- En cas de décompensation sévère :
- Polyurie
- Polydipsie
- Amaigrissement
- Prurit vulvaire/balanite
- Infections récidivantes/traînantes
Dépistage
- Par glycémie veineuse à jeun
- Quand ? :
- Sujets présentant des signes cliniques évocateurs
- Tous les sujets > 40 ans (à répéter tous les 3 ans ou plus précocement si facteurs de risque importants)
- Patients ayant un ou plusieurs facteurs de risque :
- IMC ≥ 27 kg/m²
- Parent diabétique au 1er degré
- ATCD de diabète gestationnel ou macrosomie
- HTA
- HyperTG > 2 g/L ou HDL-C < 0,35 g/L
- ATCD de diabète cortico-induit
- Obésité abdominale : > 80 (F)/94 (H) cm
- En cas d'hyperglycémie, arguments en faveur d'un DT2 : âge > 40 ans, ATCD familial de DT2, FdRV associés, IMC > 27, obésité androïde, absence de cétonurie
Diagnostics différentiels
- DT1 lent ou LADA : patient mince, pas d'ATCD familiaux, anti-IA2 et anti-GAD positifs
- Diabètes génétiques (contexte familial) :
- MODY 2 : diabète modéré du sujet jeune
- MODY 3 : diabète sévère du sujet jeune ou rapidement insulinorequérant (pseudo-type 1)
- Diabète mitochondiral : associé à une rétinite pigmentaire, une surdité
Evolution
- Aggravation de l'insulinopénie → devient insulinorequérant
- Vitesse d'aggravation fonction de l'équilibre glycémique
- Pronostic fonction des complications
Traitement
- Objectifs :
- Normalisation de l'HbA1c : < 6,5%
- Amélioration des glycémies et de l'insulinosensibilité
- Prise en charge globale des FdRV : tabac, HTA, dyslipidémie
Surveillance glycémique
- HbA1c :
- Elément essentiel
- Objectif personnalisé
- A faire tous les 3 mois
- < 7% : contrôle bon
- 7 à 8 % : à interpréter selon le contexte clinique
- > 8% : contrôle mauvais → modification thérapeutique
- Autosurveillance glycémique :
- Traitement oral :
- Pas obligatoire, nécessaire en cas de pathologie déséquilibrant le diabète ou de modification de traitement
- Outil d'éducation : sensibilisation du patient aux MHD, déterminer la posologie des médicaments hypoglycémiants, suivre l'évolution de l'insulinopénie
- 1 à 3 cycles hebdomadaires : à jeun, au réveil, à 12h avant le déjeuner et à 17h
- DT2 sous insuline :
- ASG nécessaire pour adapter les doses
- Minimum autant de glycémies capillaires que d'injections
- Traitement oral :
Règles hygiénodiététiques
- Activité physique après évaluation cardiologique :
- Exercice physique régulier : ↓ incidence DT2, amélioration de l'insulinorésistance, amélioration des chiffres tensionnels à l'effort, ↓ masse grasse
- Privilégier activités d'endurance, profiter des actes de la vie courante, intensité progressive adaptée au contexte, ne pas dépasser 50% de la FMT
- ≥ 30 min/j
- Contre-indications : insuffisance coronarienne non-stabilisée, HTA d'effort, rétinopathie proliférante non-stabilisée
- Attention à : macroprotéinurie, traitements hypoglycémiants, βB, pieds
- Alimentation :
- Régime diabétique, hypocalorique (si excès pondéral), équilibré, sans sucre d'absorption rapide
- ↓ 10% du poids, correction des TCA type grignotages
- Prise en compte des interdits, des coutumes ethniques et des contraintes professionnelles
- 50% de glucides, 30% de lipides, 20% de protides
- Glucides : éviter les sucres purs, à consommer au sein d'un repas mixte, privilégier les aliments à index glycémique bas
Traitement médicamenteux
- Associé aux règles hygiénodiététiques
Antidiabétiques oraux
| Insulinosensibilisateurs | Insulinosécréteurs | |||||||
|---|---|---|---|---|---|---|---|---|
| Biguanides | Glitazones | Sulfamides | Glinides | Inhibiteurs de la DPP IV | Inhibiteurs de l'α-glucosidase | Analogues du GLP1 | ||
| Mode d'action | ↓ insulinorésistance (hépatique) | Agonistes PPARγ ↓ insulinorésistance (adipocytaire et musculaire) |
Simulent l'insulinosécrétion | Stimulent l'insulinosécrétion Durée d'action courte (repas) |
DPPIV détruit le GLP1 ↑ insulinosécrétion en fonction de la glycémie ↓ glycémies post-prandiales |
Retardent l'absorption des glucides complexes | ↑ Insulinosécrétion liée à la glycémie | |
| Effets secondaires | Digestifs : douleurs abdominales, diarrhée → prise en milieu/fin de repas Pas de risque d'hypoglycémie Acidose lactique si non-respect des contre-indications |
Hépatiques : surveillance ASAT/ALAT tous les 2 mois la première année Prise de poids Anémie : surveillance NFS OMI Aggravation d'IC ou d'HTA |
Hypoglycémie si dosage inadapté ou IAM allergie |
Risque d'hypoglycémie (< sulfamides) Pas d'allergie croisée avec sulfamides |
Infection ORL Allergie |
Troubles digestifs (flatulences, diarrhée) → ↑ progressive des doses | Digestifs : N/V Hypoglycémies si associations aux insulinosécréteurs Insuffisance rénale | |
| Contre-indications | Age > 70 ans sauf si clairance > 60 mL/min Pathologie aiguë Insuffisance rénale Insuffisance hépatique Insuffisance cardiaque Insuffisance respiratoire |
Insuffisance rénale sévère Insuffisance hépatique Insuffisance cardiaque Grossesse, allaitement |
Grossesse et allaitement Insuffisance hépatique/rénale sévère Allergie sulfamides Association au myconazole |
Grossesse, allaitement Insuffisance hépatique |
Insuffisance rénale Insuffisance hépatique Insuffisance cardiaque |
Maladies digestives | Insuffisance rénale ATCD pancréatique | |
| Intérêt | Action sur l'insulinorésistance Pas de prise de poids Première intention sauf CI |
Association à la metformine : synergie sur l'insulinorésistance, moindre prise de poids Effet bénéfique sur la stéatose hépatique et la dyslipidémie |
Insulinosécrétion | Efficacité sur l'insulinosécrétion Pas de contre-indication jusqu'à 75 ans ou en cas d'IRC |
Pas d'hypoglycémie Utilisable chez le sujet âgé Améliore les glycémies post-prandiales Pas de prise de poids |
Utilisable chez le sujet âgé Utilisable en cas d'IRC ou d'IHC |
Amélioration des glycémies post-prandiales Pas d'hypoglycémie Perte de poids Amélioration de la dyslipidémie | |
| Effets métaboliques | -1% d'HbA1c, protection cardiovasculaire | -1% d'HbA1c | -1% d'HbA1c | -1% d'HbA1c | -0,5 à 1% d'HbA1c | -0,5 à 1% d'HbA1c | -1 à 1,5% d'HbA1c | |
Insulinothérapie
- Insulinothérapie combinée :
- Association aux hypoglycémiants oraux
- En l'absence de contre-indication aux hypoglycémiants oraux si l'insulinorequérance est partielle
- Commencer par une injection d'insuline intermédiaire type NPH au coucher ou d'analogues lents
- Adaptation progressive des doses d'insuline à la glycémie capillaire à jeun
- Intérêts : dose d'insuline facile à adapter sur la glycémie du matin, moindre prise de poids par rapport à 2 prises d'insuline
- Insulinothérapie exclusive :
- 2 à 4 injections
- Schéma basal/bolus ou mélange rapide/intermédiaire
- ASG pluriquotidienne nécessaire
- Contre-indique le renouvellement du permis poids lourds !
Stratégie thérapeutique[1]
Stratégie en cas de contre-indication à la metformine
Stratégie en cas d'allergie aux sulfamides