233 : Diabète sucré de type 1 et 2 de l’enfant et de l’adulte. Complications
De Wiki ECN
Sommaire
- 1 Objectifs
- 2 Définitions
- 3 Diabète de type 1
- 4 Diabète de type 2
- 5 Complications
- 6 Sources
Objectifs
- Diagnostiquer un diabète chez l’enfant et chez l’adulte
- Identifier les situations d’urgence et planifier leur prise en charge
- Argumenter l’attitude thérapeutique et planifier le suivi du patient
- Décrire les principes de la prise en charge au long cours
Définitions
- Glycémie :
- Normale à jeun < 1,10 g/L
- Hyperglycémie modérée à jeun : 1,10 - 1,26 g/L
- Diabète sucré :
- Glycémie à jeun ≥ 1,26 g/L à 2 reprises
- Ou glycémie aléatoire ≥ 2 g/L et signes cliniques d'hyperglycémie
| Caractéristiques | Type 1 | Type 2 |
|---|---|---|
| ATCD familiaux du même type | Rares | Fréquents |
| Age de survenue | < 35 ans | > 35 ans |
| Début | Rapide, explosif | Lent, insidieux |
| Facteur déclenchant | Souvent présent | |
| Symptomatologie | Bruyante | Pauvre/absente |
| Poids | Normal ou maigre | Obésité abdominale |
| Hyperglycémie au diagnostic | > 3 g/L | < 2 g/L |
| Cétose | Fréquente | Rare |
| Complications au moment du diagnostic | Absentes | 50% des cas |
| Cause de mortalité | Insuffisance rénale | Maladies cardiovasculaires |
Diabète de type 1
- Prévalence : 200 000 en France, gradient Nord/Sud
- Survient avant 35 ans (adolescence +++)
- Augmentation régulière de l'incidence
- Sex-ratio = 1
Physiopathologie
- Carence absolue en insuline due à la destruction des cellules β-pancréatiques
- 2 sous-types :
- Diabète type 1 auto-immun (90%) : diabète type 1 classique + LADA (Latent Autoimmune Diabetes in Adult)
- Diabète type 1 idiopathique (absence d'auto-anticorps) : diabètes cétosiques du sujet noir, diabètes suraigus japonais
Prédisposition génétique
- Toujours présente, mais pas d'ATCD familiaux dans 85% des cas
- Principaux gènes concernés : Ag de classe 2 type HLA (existe également HLA protecteurs)
- Nombreux gènes impliqués : éléments variables du gène de l'insuline, gène de la protéine CTLA-4, gène PTP-N22
Facteurs environnementaux
- Facteurs génétiques ne suffisent pas à expliquer l'étiopathogénie (50% d'atteinte commune chez les jumeaux homozygotes)
- Nombreux virus suspectés (coxsackie, CMV, rubéole, oreillons)
- Différence importante avec les facteurs précipitant le diagnostic : grippe, stress...
- Théorie hygiéniste
Processus auto-immun
- Principaux antigènes :
- Insuline et pro-insuline
- GAD (Glutamic Acid Decarboxylase)
- IA2 (islet antigen 2)
- Insulite auto-immune avec destruction des cellules β par les lymphocytes cytotoxiques
- Anticorps détectables au diagnostic :
- ICA : anticorps anti-îlots
- Anti-GAD
- Anti-IA2
- Anti-insuline
- Fréquence des autres pathologies auto-immunes associées → polyendocrinopathies auto-immunes type 1 et 2
Diagnostic
Présentation clinique initiale
- Début rapide ou explosif
- Syndrome cardinal : polyuro-polydipsie, amaigrissement, polyphagie
- Troubles visuels transitoires : jours qui suivent le début de l'insulinothérapie +++
- Fonte musculaire (quadriceps), rarement hépatomégalie
- Dyspnée de Kusmall = acidose
- Glycémie veineuse très élevée
- Glycosurie + cétonurie
- Révélation par une acidocétose inaugurale
Formes cliniques
- LADA ou diabète type 1 lent :
- Début tardif et progressif proche du type 2
- Anticorps positifs (anti-GAD +++)
- Insulinothérapie nécessaire en 2 à 10 ans
- Diabète cétosique de l'Africain :
- Début par décompensation cétosique suivie d'une possibilité d'arrêt de l'insuline dans 50% des cas après la phase aiguë
- Possibilité de répétition des épisodes de cétose avec rémission
- Anticorps négatifs
- Diagnostic tardif au stade de coma acidocétosique
- Lune de miel : période suivant le diagnostic du diabète type 1 : équilibre avec doses faibles d'insuline, parfois arrêt
Confirmation diagnostique
- Diagnostic clinique : maigreur + cétose + âge < 35 ans
- Paramètres immunologiques (si triade incomplète) : auto-anticorps ± typage HLA
- Si marqueurs immunologiques négatifs → éliminer d'autres formes de diabète proches du DT1 :
- Diabètes génétiques monogéniques : MODY, mutation du gène de l'insuline, diabètes mitochondriaux, syndrome de Wolfram (diabète insipide, diabète sucré, atrophie optique, surdité)
- Diabètes secondaires : pancréatite chronique, pancréatectomie totale, cancer du pancréas, hémochromatose, mucoviscide
- Diabète néonatal : apparition aiguë dans les 6 premiers mois, peut persister ou régresser et récidiver ; rechercher une origine non-autoimmune
- Autres causes rares :
- Inhibition fonctionnelle de l'insulinosécrétion : hypokaliémie, jeûne prolongé, phéochromocytome, somatostatinome
- Glucagonome
- Insulinorésistance primitive profonde
- Insulinorésistance secondaire : hypercorticisme, acromégalie, hyperthyroïdie
- Diabètes iatrogènes : corticoïdes, immunosuppresseurs, diurétiques hypokaliémiants, progestatifs de synthèse, salbutamol, antiprotéases du SIDA, pentamidine
Evolution
Histoire naturelle
- Modèle d'Eisenbach :
- Phase préclinique : destruction des cellules β par les processus immuns
- Diagnostic clinique : destruction > 85%
- Phase clinique séquellaire : disparition lente des cellules restantes
- Etapes :
- Prédisposition génétique
- Insulite silencieuse
- Diabète préclinique : signes métaboliques précoces, hyperglycémie
- Diabète patent peptide C + : insulinodépendance
- Diabète peptide C - : destruction totale des cellules β
Maladie chronique
- Importance de l'acceptation de la maladie par le patient
- Education : engagement permanent nécessaire du patient pour gérer le traitement et participer aux soins quotidiens
- Freins à l'adhésion :
- Peur des hypoglycémies
- Peur de prendre du poids
- Non-acceptation de la maladie
- Refus des contraintes (adolescent +++)
- Insulinothérapie inadaptée au mode de vie
- Erreurs techniques : injections trop profondes/superficielles, lipodystrophie
- Maladie surajoutée (infection +++)
- Diabète instable :
- Episodes itératifs de céto-acidoses ou hypoglycémies sévères
- Facteurs psychologiques au premier plan
Prise en charge
Principes
- Importance de l'éducation thérapeutique :
- Transfert des connaissances par enseignement collectif ou individuel
- Vérification des comportements et des acquis
- Importance des consultations infirmières et diététiques
- Définir des objectifs thérapeutiques personnalisés et acceptés :
- Réduction du risque cardiovasculaire
- Objectifs idéaux chez le diabétique type 1 non-âgé :
- Glycémie le matin à jeun : 1-1,20 g/L
- Glycémie préprandiale : 0,8-1,2
- Glycémie post-prandiale (2h) : 1,2-1,8
- Au coucher : 1,2
- A 3h du matin : > 0,8
- HbA1c ≤ 7%
- Hypoglycémies : modérées < 5/semaine, pas d'hypoglycémie sévère
- Autocontrôles : 3 à 6 par jour
- 3 à 5 injections/j
- Equilibre délicat de l'insulinothérapie :
- Diminution des complications (rétinopathie, néphropathie, neuropathie, coronaropathie) avec ↓ HbA1c
- Risque d'hypoglycémie sévère si insulinothérapie intensive
- Chez l'enfant jeune et la personne âgée : objectif d'HbA1c plus laxiste
Autosurveillance
- Buts :
- Suivre le diabète
- Adapter les doses
- Avoir une idée de l'équilibre moyen
- Gérer les situations d'urgence
- ASG ≥ 4 ×/j : pré-prandial + coucher, de temps en temps post-prandial et à 3h du matin
- Carnet d'autosurveillance
Surveillance
- Hémoglobine glyquée :
- HbA1c par méthode standardisée
- Normale : 4-6%
- Objectifs : ≤ 7%, 8% chez l'enfant et la personne âgée fragile, 8,5% avant 6 ans
- Reflet de l'équilibre glycémique sur 3 mois : glycémie moyenne (g/L) = 1,5 + (HbA1c - 7)×0,3
- Causes d'erreur de mesure : anémie hémolytique, urémie, hémoglobinopathie, traitement par EPO, saignées → fructosamine
- Bilan métabolique annuel : EAL, créatinine, microalbuminurie, ECBU, ECG
- Dépistage FO annuel
- Consultation spécialisée tous les 3 à 4 mois
Insulinothérapie
- Traitement principal, palliatif, à vie
- Variétés :
- Insuline recombinante : identique à l'insuline humaine
- Insulines rapides : Actrapid, Insuman
- Insulines ralenties : NPH, Ultraltard
- Analogues de l'insuline : structure modifiée à but thérapeutique
- Analogues rapides (juste avant le repas) : Humalogue, Novorapid
- Analogues lents (1 à 2 fois par jour à heure fixe) : Lantus, Levemir
- Parfois mélanges préconditionnés
- Insuline recombinante : identique à l'insuline humaine
- Résorption cutanée dépend de la profondeur, de la zone, de la dose, de l'environnement thermique et de l'activité musculaire du membre concerné
- 2 modes d'administration :
- Stylos à insuline (réutilisables ou UU)
- Pompes portables pour administration continue modulée : plus efficaces mais plus contraignantes et chères
- Schémas :
- Choix selon acceptation, autonomisation, objectifs thérapeutiques
- Schéma basal-bolus : analogues lents couvrant le nycthémère + analogues rapides avant les repas
- 4 injections : 3 rapides pré-prandiales, 1 lente pour couvrir la nuit
- 3 injections : regroupement injection lente et rapide du soir
- Doses en général < 1 UI/kg, à adapter en fonction des glycémies, de l'activité physique et de l'alimentation prévues
- Education thérapeutique pour l'auto-gestion +++ (insulinothérapie fonctionnelle)
- Effets secondaires :
- Hypoglycémies
- Prise de poids : +5 kg en moyenne
- Allergie (rare)
- Lipoatrophie d'origine immunologique
- Lipohypertrophie si piqûre au même endroit
Traitement non-insulinique
- Maladie chronique → suivi multidisciplinaire, consultation d'annonce, soutien et accompagnement
- Alimentation variée sans interdit mais horaires et apports glucidiques réguliers
- Exercice physique
- Associations de patients
Cas particuliers
Diabète de l'enfant et de l'adolescent
- Fréquence des acido-cétoses
- Attention aux hypoglycémies sévères, surtout chez le jeune enfant
- Diabète difficile à équilibrer : ↑ des besoins en insuline, acceptation difficile
- Part croissante de diabète de type 2 chez les enfants obèses
Diabète chez la femme
- Diabète gestationnel
- Contraception : contre-indication aux estroprogestatifs et des progestatifs dérivés des norstéroïdes
- Grossesse :
- Pronostic normal si équilibre périconceptionnel parfait et jusqu'à l'accouchement
- Utiliser des analogues de l'insuline ayant l'AMM chez la femme enceinte
- Retentissement de la grossesse sur le diabète :
- Baisse physiologique de l'HbA1c
- ↑ des besoins en fin de grossesse, ↓ en post-partum
- Risque d'aggravation de la rétinopathie et de la néphropathie si non-stabilisées
- Contre-indication absolue : insuffisance coronaire
- Objectifs glycémiques stricts, suivi rapproché spécialisé mensuel
- Ménopause : éviter l'hormonothérapie substitutive percutanée
Personne âgée
- Ne pas craindre l'insulinothérapie
- Objectifs plus laxistes chez les personnes fragiles à haut risque hypoglycémique
Diabète et jeûne
- Ne jamais arrêter l'insuline en cas d'intolérance alimentaire, essayer des collations liquides fractionnées ou administration de glucose IV
- Vérifier la cétonurie et la cétonémie : troubles digestifs peuvent révéler une cétose
- Hospitalisation systématique en cas de nécessité de jeûne > 1h avec perfusion glucosée et adaptation des doses d'insuline
- Jeûne prolongé nécessaire : insuline IVSE + glucosé IV
Diabète de type 2
- 85% des diabètes, prévalence ~4%
- Prévalence augmente avec l'âge
- Prévalence augmente de 5%/an
- Personnes à risque : obèses, anomalies du métabolisme glucidique, ATCD familiaux de DT2, ethnies (noirs, hispaniques)
- Découvert en général à l'âge adulte
- Insulinorésistance initialement répondant aux antidiabétiques oraux (ADO), insulinorequérance secondaire
Physiopathologie
- Elément central = diminution de la sensibilité à l'insuline, favorisée par l'obésité androïde, l'âge et la sédentarité
- Insulinorésistance :
- Incapacité de l'insuline d'atteindre une réponse maximale au niveau des organes cibles
- Défaut de captation musculaire du glucose
- Accroissement de production de glucose au niveau hépatique → hyperglycémie à jeun
- Insulinopénie relative : insuffisance de sécrétion d'insuline par rapport au niveau de la glycémie
- Facteurs génétiques : si les 2 parents sont diabétiques, 30 à 60% de chance pour le sujet de le devenir
- Glucotoxicité : hyperglycémie aggrave le déficit d'insulinosécrétion et l'insulinorésistance par élévation du seuil du glucose sensor
- Lipotoxicité : insulinopénie → non-freination de la lipolyse → ↑ acides gras libres → diminue l'insulinosécrétion
- Syndrome métabolique lié +++ à l'insulinorésistance :
- Obésité abdominale (PA > 102 (H)/88 (F) cm)
- Hypertriglycéridémie
- ↓ HDL
- HTA
- Hyperglycémie modérée à jeun, voire diabète
Diagnostic
Clinique
- En général, évolution asymptomatique ou à bas bruit
- En cas de décompensation sévère :
- Polyurie
- Polydipsie
- Amaigrissement
- Prurit vulvaire/balanite
- Infections récidivantes/traînantes
Dépistage
- Par glycémie veineuse à jeun
- Quand ? :
- Sujets présentant des signes cliniques évocateurs
- Tous les sujets > 40 ans (à répéter tous les 3 ans ou plus précocement si facteurs de risque importants)
- Patients ayant un ou plusieurs facteurs de risque :
- IMC ≥ 27 kg/m²
- Parent diabétique au 1er degré
- ATCD de diabète gestationnel ou macrosomie
- HTA
- HyperTG > 2 g/L ou HDL-C < 0,35 g/L
- ATCD de diabète cortico-induit
- Obésité abdominale : > 80 (F)/94 (H) cm
- En cas d'hyperglycémie, arguments en faveur d'un DT2 : âge > 40 ans, ATCD familial de DT2, FdRV associés, IMC > 27, obésité androïde, absence de cétonurie
Diagnostics différentiels
- DT1 lent ou LADA : patient mince, pas d'ATCD familiaux, anti-IA2 et anti-GAD positifs
- Diabètes génétiques (contexte familial) :
- MODY 2 : diabète modéré du sujet jeune
- MODY 3 : diabète sévère du sujet jeune ou rapidement insulinorequérant (pseudo-type 1)
- Diabète mitochondiral : associé à une rétinite pigmentaire, une surdité
Evolution
- Aggravation de l'insulinopénie → devient insulinorequérant
- Vitesse d'aggravation fonction de l'équilibre glycémique
- Pronostic fonction des complications
Traitement
- Objectifs :
- Normalisation de l'HbA1c : < 6,5%
- Amélioration des glycémies et de l'insulinosensibilité
- Prise en charge globale des FdRV : tabac, HTA, dyslipidémie
Surveillance glycémique
- HbA1c :
- Elément essentiel
- Objectif personnalisé
- A faire tous les 3 mois
- < 7% : contrôle bon
- 7 à 8 % : à interpréter selon le contexte clinique
- > 8% : contrôle mauvais → modification thérapeutique
- Autosurveillance glycémique :
- Traitement oral :
- Pas obligatoire, nécessaire en cas de pathologie déséquilibrant le diabète ou de modification de traitement
- Outil d'éducation : sensibilisation du patient aux MHD, déterminer la posologie des médicaments hypoglycémiants, suivre l'évolution de l'insulinopénie
- 1 à 3 cycles hebdomadaires : à jeun, au réveil, à 12h avant le déjeuner et à 17h
- DT2 sous insuline :
- ASG nécessaire pour adapter les doses
- Minimum autant de glycémies capillaires que d'injections
- Traitement oral :
Règles hygiénodiététiques
- Activité physique après évaluation cardiologique :
- Exercice physique régulier : ↓ incidence DT2, amélioration de l'insulinorésistance, amélioration des chiffres tensionnels à l'effort, ↓ masse grasse
- Privilégier activités d'endurance, profiter des actes de la vie courante, intensité progressive adaptée au contexte, ne pas dépasser 50% de la FMT
- ≥ 30 min/j
- Contre-indications : insuffisance coronarienne non-stabilisée, HTA d'effort, rétinopathie proliférante non-stabilisée
- Attention à : macroprotéinurie, traitements hypoglycémiants, βB, pieds
- Alimentation :
- Régime diabétique, hypocalorique (si excès pondéral), équilibré, sans sucre d'absorption rapide
- ↓ 10% du poids, correction des TCA type grignotages
- Prise en compte des interdits, des coutumes ethniques et des contraintes professionnelles
- 50% de glucides, 30% de lipides, 20% de protides
- Glucides : éviter les sucres purs, à consommer au sein d'un repas mixte, privilégier les aliments à index glycémique bas
Traitement médicamenteux
- Associé aux règles hygiénodiététiques
Antidiabétiques oraux
| Insulinosensibilisateurs | Insulinosécréteurs | |||||||
|---|---|---|---|---|---|---|---|---|
| Biguanides | Glitazones | Sulfamides | Glinides | Inhibiteurs de la DPP IV | Inhibiteurs de l'α-glucosidase | Analogues du GLP1 | ||
| Mode d'action | ↓ insulinorésistance (hépatique) | Agonistes PPARγ ↓ insulinorésistance (adipocytaire et musculaire) |
Simulent l'insulinosécrétion | Stimulent l'insulinosécrétion Durée d'action courte (repas) |
DPPIV détruit le GLP1 ↑ insulinosécrétion en fonction de la glycémie ↓ glycémies post-prandiales |
Retardent l'absorption des glucides complexes | ↑ Insulinosécrétion liée à la glycémie | |
| Effets secondaires | Digestifs : douleurs abdominales, diarrhée → prise en milieu/fin de repas Pas de risque d'hypoglycémie Acidose lactique si non-respect des contre-indications |
Hépatiques : surveillance ASAT/ALAT tous les 2 mois la première année Prise de poids Anémie : surveillance NFS OMI Aggravation d'IC ou d'HTA |
Hypoglycémie si dosage inadapté ou IAM allergie |
Risque d'hypoglycémie (< sulfamides) Pas d'allergie croisée avec sulfamides |
Infection ORL Allergie |
Troubles digestifs (flatulences, diarrhée) → ↑ progressive des doses | Digestifs : N/V Hypoglycémies si associations aux insulinosécréteurs Insuffisance rénale | |
| Contre-indications | Age > 70 ans sauf si clairance > 60 mL/min Pathologie aiguë Insuffisance rénale Insuffisance hépatique Insuffisance cardiaque Insuffisance respiratoire |
Insuffisance rénale sévère Insuffisance hépatique Insuffisance cardiaque Grossesse, allaitement |
Grossesse et allaitement Insuffisance hépatique/rénale sévère Allergie sulfamides Association au myconazole |
Grossesse, allaitement Insuffisance hépatique |
Insuffisance rénale Insuffisance hépatique Insuffisance cardiaque |
Maladies digestives | Insuffisance rénale ATCD pancréatique | |
| Intérêt | Action sur l'insulinorésistance Pas de prise de poids Première intention sauf CI |
Association à la metformine : synergie sur l'insulinorésistance, moindre prise de poids Effet bénéfique sur la stéatose hépatique et la dyslipidémie |
Insulinosécrétion | Efficacité sur l'insulinosécrétion Pas de contre-indication jusqu'à 75 ans ou en cas d'IRC |
Pas d'hypoglycémie Utilisable chez le sujet âgé Améliore les glycémies post-prandiales Pas de prise de poids |
Utilisable chez le sujet âgé Utilisable en cas d'IRC ou d'IHC |
Amélioration des glycémies post-prandiales Pas d'hypoglycémie Perte de poids Amélioration de la dyslipidémie | |
| Effets métaboliques | -1% d'HbA1c, protection cardiovasculaire | -1% d'HbA1c | -1% d'HbA1c | -1% d'HbA1c | -0,5 à 1% d'HbA1c | -0,5 à 1% d'HbA1c | -1 à 1,5% d'HbA1c | |
Insulinothérapie
- Insulinothérapie combinée :
- Association aux hypoglycémiants oraux
- En l'absence de contre-indication aux hypoglycémiants oraux si l'insulinorequérance est partielle
- Commencer par une injection d'insuline intermédiaire type NPH au coucher ou d'analogues lents
- Adaptation progressive des doses d'insuline à la glycémie capillaire à jeun
- Intérêts : dose d'insuline facile à adapter sur la glycémie du matin, moindre prise de poids par rapport à 2 prises d'insuline
- Insulinothérapie exclusive :
- 2 à 4 injections
- Schéma basal/bolus ou mélange rapide/intermédiaire
- ASG pluriquotidienne nécessaire
- Contre-indique le renouvellement du permis poids lourds !
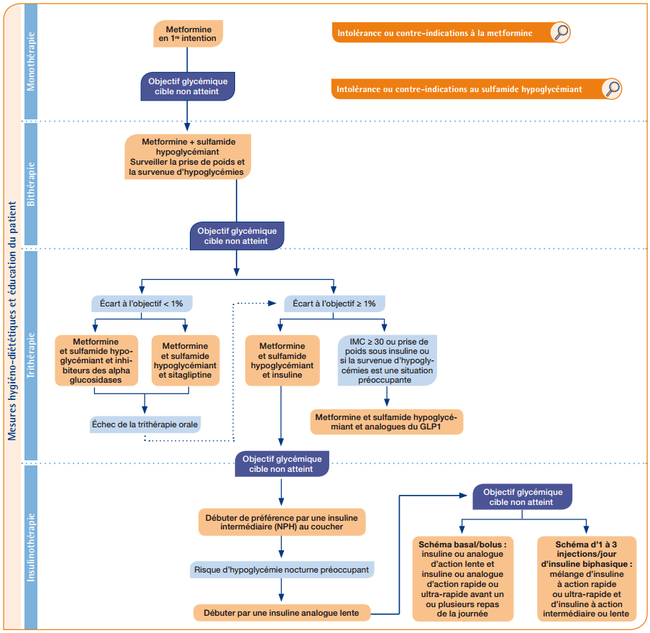
Stratégie thérapeutique[1]
Stratégie en cas de contre-indication à la metformine
Stratégie en cas d'allergie aux sulfamides
Suivi
- Recherche d'atteinte d'organes cibles : oculaires, rénales, neurologiques, cardiovasculaires, lésions des pieds
- Examens complémentaires :
- FO annuel avec dilatation
- ECG de repos annuel
- Risque cardiovasculaire élevé → bilan cardiologique à la recherche d'ischémie myocardique asymptomatique
- Echo-Doppler des membres inférieurs avec calcul de l'IPS : patients > 40 ans ou diabète > 20 ans, à faire tous les 5 ans ou sur point d'appel clinique +++
- Suivi biologique :
- HbA1c 4×/an
- Glycémie veineuse à jeun pour contrôler l'ASG, annuellement
- Bilan lipidique annuel
- Recherche de microalbuminurie annuelle
- Créatininémie annuelle avec calcul de clairance
- TSH si signes cliniques
Complications
Rétinopathie diabétique
- Complication chronique de l'hypoglycémie →
- DT1 : absente au diagnostic, mais 80% après 15 ans d'évolution
- DT2 : 20% au diagnostic, > 50% après 15 ans d'évolution
- Prévalence augmente avec la durée du diabète et le mauvais contrôle glycémique
- Première cause de cécité en France chez les moins de 50 ans
- Evolution perfide, BAV tardive
- Accessible à la prévention
- Menace : prolifération de néovaisseaux
- Maculopathie non-systématique
Physiopathologie
- Souffrance endothéliale → épaississement de la membrane basale → formation de zones d'ischémie et d'œdème
- Phénomènes occlusifs et ischémiques en périphérie :
- Tendance évolutive vers l'extension
- Prolifération de néovaisseaux dans la rétine et le vitré
- Risque d'hémorragie intravitréenne, de décollement de rétine, de glaucome néovasculaire et de rubéose irienne
- Phénomènes œdémateux maculaires :
- Exsudats
- Œdème maculaire non-cystoïde puis cystoïde
Diagnostic
- Fond d’œil
- Microanévrismes : hémorragies punctiformes prédominant au pôle postérieur, pas de traduction fonctionnelle
- Nodules cotonneux
- Signes préprolifératifs :
- Hémorragies intrarétiniennes en tache : taille plus grande que les punctiformes
- Dilatation veineuse irrégulière en chapelet
- Anomalies microvasculaires intrarétiniennes (AMIR) : dilatations et télangiectasies vasculaires (néovaisseaux dans l'épaisseur de la rétine)
- Signes de néovascularisation :
- Néovaisseaux prérétiniens et prépapillaires
- Hémorragie prérétinienne ou intravitréenne (BAV) avec risque de décollement de rétine par traction lors de sa résorption
- Lésions maculaires :
- Œdème maculaire
- Aspect cystoïde : cas sévères
- Exsudats : aspect sévère = placard exsudatif centromaculaire
- Examens complémentaires spécialisés :
- Angiographie à la fluorescéine : préciser le stade et l'évolutivité au moment du diagnostic, visualisation des zones ischémiques et de perméabilité capillaire
- Tomographie en cohérence optique (OCT) : détecter l’œdème maculaire
- Classification
| Stade | Lésions | Altération de la vision | Traitement |
|---|---|---|---|
| Non-proliférante | Dilatation capillaire Microanévrismes Exsudats Hémorragies Rares AMIR |
Non | Normalisation glycémique Contrôle tensionnel |
| Préproliférante ou proliférante | Nombreuses zones d'ischémie Hémorragies rétiniennes en taches AMIR Néovaisseaux |
Possible | Contrôle tensionnel Panphotocoagulation au LASER Normalisation glycémique prudente |
| Proliférante compliquée | Hémorragie du vitré Décollement de rétine |
Oui | Normalisation glycémique Contrôle tensionnel Panphotocoagulation Chirurgie |
| Maculopathie | Œdème maculaire | Oui | Normalisation glycémique Contrôle tensionnel Photocoagulation au LASER |
Dépistage
- Examen ophtalmologique dès le diagnostic
- Puis tous les ans
- Etudie :
- Acuité visuelle
- Pression intraoculaire (risque de glaucome)
- Cristallin (risque de cataracte)
- FO après dilatation
- Angiographie si lésions au FO
- Possibilité de dépistage par photographie de FO avec lecture différée en centre de référence[2]
- Situations nécessitant une surveillance rapprochée :
- Adolescence
- Grossesse : programmation de la grossesse, FO préalable + surveillance trimestrielle
- Après plusieurs années de mauvais contrôle : modérer les objectifs glycémiques à court terme en cas de rétinopathie importante
- Chirurgie de la cataracte : risque d'aggravation, mais possibilité également de meilleure évaluation
Traitement
- Equilibre glycémique et tensionnel
- Panphotocoagulation rétinienne :
- En ambulatoire, progressivement
- Action sur la néovascularisation +++, plus difficile pour la maculopathie
- Formes sévères ou saignement persistant : injection intraoculaire de VEGF
- Chirurgie : vitrectomie avec laser peropératoire
Autres complications oculaires
- Cataracte
- Glaucome néovasculaire
- Paralysies oculomotrices isolées (III, IV ou VI) : manifestation de mononeuropathie diabétique, régression spontanée en quelques mois
Néphropathie diabétique
- Première cause d'insuffisance rénale terminale en Europe
- Augmente +++ le risque cardiovasculaire des diabétique
Physiopathologie
- Atteinte glomérulaire avec élévation de la pression intraglomérulaire secondaire à la souffrance endothéliale (vasoplégie des artérioles afférentes)
- ↑ pression intraglomérulaires → dilatation des glomérules → meilleure filtration à court terme
- Adaptation glomérulaire = épaississement de la membrane basale et prolifération de cellules mésangiales
- Altération progressive de la qualité du filtre glomérulaire → laisse passer de l'albumine toxiques pour les segments distaux
- Sclérose glomérulaire → ↓ DFG
- Différences génétiques de sensibilité à la NPD
Dépistage
- Dépistage annuel :
- BU (recherche de protéinurie et d'hématurie/infection faussant les résultats) + microalbuminurie (sur échantillon ou des 24h) si BU négative
- Microalbuminurie ou protéinurie doit être confirmée à 2 reprises (1 dépistage + 2 confirmations)
- Si confirmée → quantification sur échantillon de 24h
- Risque de faux positif de microalbuminurie :
- Orthostatisme prolongé
- Activité physique intense
- Tabagisme
- Fièvre
- Poussée d'IC
- Hyperglycémie marquée
- Infection urinaire
- Menstruations
Diagnostic
- Diagnostic histologique, mais PBR rarement pratiquée
- En présence d'une rétinopathie et d'une excrétion urinaire d'albumine progressivement croissante, diagnostic de NPD retenu
- PBR = en cas de situations atypiques :
- Absence de rétinopathie
- Apparition précoce (< 10 ans) chez un DT1
- Aggravation rapide
- HTA sévère, protéinurie non-sélective, syndrome néphrotique à un stade précoce
- Hématurie
- En cas d'HTA difficilement contrôlée/se majorant rapidement : recherche de sténose de l'artère rénale (attention au PdCI)
- Plus fréquente chez les diabétique
- Aggravation de la fonction rénale sous bloqueur du SRAA
- Classification :
| Stade 1 Hypertrophie et hyperfiltration |
Stade 2 Phase silencieuse |
Stade 3 Néphropathie incipiens |
Stade 4 Néphropathie |
Stade 5 Insuffisance rénale | |
|---|---|---|---|---|---|
| Années après le diagnostic | 1 | 2 à 6 | 7 à 15 | 15 à 20 | > 20 |
| Albuminurie | Normale | Normale | Microalbuminurie (30-300 mg/j) | Protéinurie (> 0,3 g/j) | Protéinurie massive |
| Pression artérielle | Normale | Normale | Discrètement augmentée Perte de la baisse nocturne |
Elevée | Elevée |
| Filtration glomérulaire | Elevée | Elevée à normale | Normale | -10 mL/min/an sans traitement | Effondrée |
Traitement
Au stade de microalbuminurie
- Contrôle glycémique : HbA1c < 6,5%
- Contrôle tensionnel < 130/80 mmHg
- Bloqueurs du SRAA : IEC ou ARAII
- Prise en charge globale :
- Prise en charge des FdRV (statine et aspirine +++)
- Régime hypoprotidique à 0,8 g/kg/j
- Limiter les néphrotoxiques : AINS, PdCI (précautions)
Au stade de macroalbuminurie
- Priorité = contrôle tensionnel < 130/80 mmHg → IEC/ARAII + thiazidique ± βB ± anticalcique
- Prise en charge des complications au stade d'IRC :
- Anomalies phosphocalciques
- Anémie arégénérative (plus précoce chez le diabétique)
- Préparation au traitement de suppléance
Risque infectieux
- Infections plus fréquentes, 90% asymptomatiques favorisées par la neuropathie vésicale
- Dépistage par BU annuelle
- Conséquences :
- Risque d'infection urinaire haute : PNA compliquée, nécrose papillaire, pyélonéphrite emphysémateuse rare
- Risque d'aggravation d'une néphropathie glomérulaire débutante, ou d'aggravation avancée
- Traitement :
- Infection symptomatique → comme toute infection urinaire
- Infection asymptomatique → pas de consensus, ne pas traiter systématiquement
- 70% de récidives
Neuropathie diabétique
- 50% des diabétiques après 20 ans d'évolution
- Facteurs favorisants :
- Grande taille
- Tabagisme
- Age
- Présence d'AOMI
- Carences nutritionnelles ou vitaminiques
- Alcool
- Atteinte double :
- Neurotoxicité directe de l'hyperglycémie chronique
- Atteinte vasculaire par oblitération des vasa vasorum
Diagnostic
- Neuropathie débutante souvent silencieuse → recherche active
- Importance de l'examen des pieds
Neuropathie sensorimotrice
- Atteinte des fibres les plus longues en premier → chaussettes et gants ; rarement bandes
- Petites fibres : sensibilité thermo-algique et tact épicritique
- Grosses fibres : proprioception, pallesthésie, force motrice
- EMG souvent inutile !
- Polynévrite symétrique distale :
- La plus fréquente
- Chronique, progressive, régression rare
- Paresthésies distales remontant lentement en proximal
- Douleurs : atroces, sensation d'arc électrique, d'écrasement, de brûlure
- Hypoesthésie (plaies et cors indolores +++)
- Réflexes achilléens voire rotuliens abolis
- Déformation du pied : de la voûte plantaire, des orteils, avec positions vicieuses et points d'appui anormaux
- A l'extrême : pied de Charcot presque parallélépipédique, déminéralisation du tarse en radio
- Polynévrite asymétrique proximale = amyotrophie diabétique :
- Forme rare type radiculopathie L2, L3 ± L4
- Cruralgie + fatigabilité douloureuse proximale, évolution stable
- Amyotrophie +++
- Polyradiculopathie thoracique : rare, douleurs abdominales entre niveaux T4 et T12, retard diagnostique fréquent
- Mononévrites :
- Aiguës, asymétriques
- Nerfs crâniens le plus souvent : VI, III, IV, VII
- Membres supérieurs rarement touchés, plutôt neuropathie compressive type canal carpien bilatéral
- Multinévrites : plusieurs nerfs en général d'un seul côté, rares, rechercher une vascularite
Neuropathie autonome
- Complication d'un diabète ancien, régression rare
- Neuropathie autonome cardiovasculaire :
- Tachycardie sinusale quasi-permanente autour de 110 bpm variant peu à l'effort
- Rares bradycardies permanentes
- Allongement du QT
- Risque d'ischémie silencieuse
- Neuropathie autonome vasomotrice :
- Hypotension orthostatique sans accélération du pouls, peut être favorisée par des traitements antihypertenseurs
- Trouble de la microcirculation périphérique → hyperémie, rougeur, œdème, troubles sudoraux
- Troubles de la sudation :
- Anomalie de la régulation nerveuse
- Anhidrose des membres inférieurs → sécheresse cutanée, risque d'hyperkératose, cors et plaies
- Parfois hyperhidrose de la partie supérieure du corps
- Complications : prurit, lésions de grattage qui peuvent s'impétiginiser, dépilation
- Neuropathie digestive :
- Parésie du tractus digestif
- Dysphagie
- Gastroparésie : satiété rapide, pesanteur abdominale, régurgitations/vomissements, souvent peu symptomatique, à évoquer si hypoglycémies paradoxales post-prandiales
- Diarrhée banale ou motrice d'évolution capricieuse, éliminer d'autres causes
- Constipation (rechercher un cancer colorectal si alternance diarrhée/constipation)
- Rare incontinence fécale
- Neuropathie vésicale :
- Défaut de perception de la plénitude vésicale + hypoactivité du détrusor
- Favorisée par la polyurie de l'hyperglycémie
- Résidu mictionnel permanent → risque d'incontinence urinaire, de RAU, d'infection et de retentissement sur le haut appareil
- Evaluation clinique et échographique de la prostate +++, bilan urodynamique, échographie vésicale post-mictionnelle
- Dysfonction érectile :
- Participation psychologique
- Rares syndromes de Leriche
- Neuropathie + fibrose des corps caverneux
- Penser aux diagnostics différentiels
Moyens diagnostiques
- Diagnostic clinique :
- Interrogatoire : signe d'hypotension orthostatique, diarrhée, douleurs, paresthésies...
- Inspection des pieds
- Recherche des ROT
- Test au monofilament , coter le nombre d'applications détectées
- Tester la sensibilité épicritique, thermoalgique, pallesthésique et proprioceptive
- ECG annuel
- EMG : seulement si atypie de la neuropathie ou absence d'autre complication (rétinopathie +++)
- Etude de la variation du rythme cardiaque à l'effort
- Gastroparésie vue en fibroscopie : persistance du bol alimentaire voire bézoard
- Mesure échographique du RPM, bilan urodynamique
- Recherche de dénervation cardiaque sympathique :
- Variations de la FC lors de la respiration profonde : enregistrement ECG en respiration profonde après 15 min de repos, anormale si variation < 10
- Manœuvre de Valsalva avec mesure du rapport entre RR le plus long et le plus court, N > 1,20, contre-indiquée si rétinopathie proliférante
- Test d'hypotension artérielle orthostatique avec mesure de la variation de FC
Diagnostic différentiel
- Neuropathies métaboliques : insuffisance rénale, amylose, hypothyroïdie
- Neuropathies toxiques : alcool, tabac, chimiothérapie, isoniazide
- Neuropathies paranéoplasiques : cancers bronchiques, gastriques, et lymphomes
- Neuropathies carentielles : thiamine, pyridoxine, B6, B12
- Neuropathies inflammatoires : Guillain-Barré, polynévrite chronique inflammatoire démyélinisante idiopathique
- Infection : lèpre, Lyme
- Autres : Charcot-Marie-Tooth, PAN
Traitement
- Préventif : équilibre glycémique, prise en charge des facteurs favorisants (alcool, tabac, insuffisance rénale, médicaments)
- Prévention des complications une fois la neuropathie installée (mal perforant plantaire +++)
- Traitement symptomatique :
- Antalgiques traditionnels et contre les douleurs neuropathiques (BZD, antiépileptiques, ATD)
- Hydratation des tissus cutanés : crème, pommade
- Traitement mécanique des hyperkératoses = pédicurie
Macroangiopathie
- Athérosclérose accélérée
- Complications vasculaires plus sévères (IDM plus souvent mortels)
- Association à une calcification diffuse de la média : médiacalcose
- Mortalité cardiovasculaire = principale cause de mortalité des DT2 (coronaire ×3, AVC × 2, AOMI ×10)
- Physiopathologie : voir FdRV
Dépistage
- Approche globale → risque de décès cardiovasculaire à 10 ans
- Identifier les facteurs de risque :
- Age, durée du diabète (> 10 ans +++), ATCD familiaux cardiovasculaires précoces
- Tabagisme
- HTA
- HDL < 0,4 g/L et LDL > 1,6 g/L
- Microalbuminurie > 30 mg/24h
- Obésité abdominale (102 H/88 F), obésité (IMC > 30 kg/m²)
- Consommation excessive d'alcool
- Sédentarité
- Aspects psychosociaux
- Rechercher une atteinte artérielle :
- Coronaire :
- ECG de repos annuel
- Si signes cliniques ou ECG évocateurs : épreuve d'effort, scintigraphie myocardique, voire coronarographie
- Recherche d'ischémie silencieuse
- Carotidienne :
- Auscultation à chaque consultation
- EDTSA si symptomatologie évocatrice d'AIT voire systématique tous les 3 ans si HTA
- AOMI :
- Inspection des pieds, palpation des pouls, auscultation des trajets artériels
- Recherche de claudication
- Mesure de l'IPS mais attention à la médiacalcose
- EDAMI
- Coronaire :
Diagnostic
- Fréquence des ischémies myocardiques silencieuses
- Penser systématiquement à un IDM devant la survenue de symptômes inexpliqués : troubles digestifs, douleur épigastrique, asthénie à l'effort, TdR, embolie, baisse de la PA
- Dépistage systématique si risque CV élevé
- Situations à risque vasculaire extrême :
- Diabétique avec microangiopathie sévère, protéinurie > 1 g/L
- Diabétique avec atteinte vasculaire avérée
- AOMI :
- Risque de forme atténuée par neuropathie concomitante
- Risque élevé de gangrène même quand les pouls distaux sont conservés
- Gangrène témoigne toujours d'une macroangiopathie → revascularisation +++ car même en cas d'amputation, risque de non-cicatrisation
Traitement
- Prévention primaire et secondaire
- Revascularisation : risque de sténose important → stent systématique sur les coronaires, place importante du pontage
- Contrôle glycémique :
- Objectif d'HbA1c < 7% (6,5% si sujet jeune)
- Rôle +++ de la metformine chez les obèses
- Importance du contrôle glycémique en phase aiguë (SCA, AVC) pour le pronostic
- Activité physique :
- Systématiquement recommandée à un niveau adapté au patient
- Réintroduction en général, 30 minutes 3 fois/semaine
- Si suspicion de coronaropathie latente : épreuve d'effort préalable ± scintigraphie myocardique
- Contrôle lipidique :
- Objectifs de LDL-C :
- Aucun risque additionnel, évolution < 5 ans, pas de microangiopathie : < 1,9 g/L
- ≤ 1 FdRV : < 1,6 g/L
- ≥ 2 autres FdRV et diabète < 10 ans : < 1,3 g/L
- Prévention secondaire ou atteinte rénale ou diabète > 10 ans ou > 2 FdRV : < 1 g/L
- Moyens : intensification du traitement du diabète, régime pauvre en graisses animales, ± statine
- Objectifs de LDL-C :
- Contrôle tensionnel :
- Objectif < 130/80 mmHg
- MHD + traitement antihypertenseur si échec : βB, IEC, ARAII, inhibiteur calcique, thiazidiques
- Prévention du risque thrombotique : AAP type aspirine si ≥ 1 FdRV associé
- Maîtrise pondérale : IMC < 25 kg/m², tour de taille < 94 (H)/80 (F) cm
- Sevrage tabagique
Pied diabétique
- Artériopathie + neuropathie +++
- Du mal perforant plantaire (neuropathie pure) à l'ischémie aiguë d'orteil ou de membre (artériopathie pure)
- Complication : risque d'infection+++
- Patients à risque podologique élevé :
- Artéritiques : pouls abolis
- Troubles de la statique du pied
- Trouble de la sensibilité algique, vibratoire, thermique, profonde
- ATCD d'ulcération au niveau des pieds
- Stades :
- Grade 0 : absence de neuropathie sensitive et d'artériopathie
- Grade 1 : neuropathie sensitive isolée
- Grade 2 : association neuropathie + artériopathie ou neuropathie + déformation des pieds
- Grade 3 : ATCD d'ulcération ou d'amputation
Formes cliniques
- Mal perforant plantaire :
- Neuropathie → hypoesthésie + déformations articulaires
- Points d'appuis normaux : 5 têtes des métatarsiens + styloïde du 5ème métatarsien + talon
- Au niveau des points d'appui, développement de durillon qui peuvent évoluer vers le MPP
- Pression permanente excessive → hyperkératose réactionnelle → durillons
- Durillon + hypoesthésie → pas de douleur → à chaque appui, tissus mous écrasés entre l'os et le durillon → dilacération → formation de collections
- Soins inadaptés + sécheresse du durillon → fissures du durillon → porte d'entrée infectieuse vers la collection → abcès sous le durillon → risque d'ostéite
- Manifestation révélatrice :
- Pus va sourdre des fissures → tache la chaussette
- Inflammation de la zone autour du durillon
- Fusée plantaire : zone inflammatoire par propagation du pus le long d'une gaine aponévrotique
- Cellulite de révélation bruyante avec signes généraux
- Ischémie/nécrose noire :
- Obstruction ou sténose des artères de petit et moyen calibre
- Peau froide, dépilée, fine, livedo
- Moindre plaie va induire une nécrose
- Urgence = revascularisation
- Lésions complexes : MPP + nécrose, nécessité de revascularisation en urgence, risque de surinfection +++
- Gangrène ou cellulite extensive :
- Terrain artériel, urgence infectieuse vitale, tableau septique +++
- Gangrène gazeuse : C. perfringens, crépitations à la palpation, clartés des parties molles à la radio → amputation en urgence vitale + réanimation + ATB
Conduite à tenir en urgence
- Bilan lésionnel initial :
- Dater l'apparition de la lésion, qualifier en neuropathie ou artériopathie
- Localiser la plaie, vérifier sa couleur
- Rechercher des signes locaux de diffusion (lymphangite, fusée plantaire, érysipèle...)
- Vérifier les signes généraux et coter la douleur
- Examens de première intention :
- Radiographie de pied centrée sur la zone atteinte, bilatérale
- Hémogramme, ionogramme sanguin, créatinine, CRP, hémocultures si fièvre
- Surveillance : pouls, PA, température, diurèse, glycémie horaire
- Traitement d'urgence :
- Décharge systématique
- Parage de la lésion, excision de l'hyperkératose pour bilan lésionnel, prélèvement profond, rechercher un contact osseux avec stylet pointe mousse
- Antibiothérapie si infection clinique
- Anticoagulation préventive
- Antalgie efficace
- Insulinothérapie IVSE si mauvais équilibre
- Matelas anti-escarre
- SAT-VAT
Principes de traitement
- Décharge de toutes les plaies : proscrire l'appui, chaussures adaptées
- Détersion manuelle de l'hyperkératose
- Revascularisation si participation artériopathique
- ATB si plaie infectée cliniquement : CGP sur plaie récente, BGN si traînante ; durée de 15 jours
- Ostéite : diagnostic radiologique (répéter les radio), recherche de contact osseux à la pointe mousse +++, traitement = résection chirurgicale ou ATB 12 semaines
Education du patient
- Patient diabétique sans risque :
- Bon équilibre glycémique
- Prise en charge des FdRV (tabac +++)
- Patient à risque :
- Protection des pieds : ne pas marcher pieds nus, poncer les cors (ne pas les entailler), pas de substance corosice, pas de bouillotte pour réchauffer les pieds
- Inspection quotidienne des pieds
- Vérifier l'absence de corps étranger dans les chaussures
- Laver les pieds tous les jours à l'eau et bien les sécher
- Hydratation quotidienne des pieds si sécheresse
- Soins de pédicurie réguliers
- Chaussures adaptées
- Changer les chaussettes tous les jours
- Eviter les élastiques serrant le mollet
Complications dentaires
- Risque élevé de maladie parodontale
- Inflammation grave destructrice des gencives, cause de pertes de dents +++
- Nettoyages trop peu fréquents → accumulation de bactéries dans le sillon gingival → formation de plaque dentaire → toxines et tarte → désolidarisation de la gencive et de la dent
- Risque également d'abcès dentaires, surtout si diabète déséquilibré
- Facteurs favorisants :
- Diabétiques produisent plus de plaque dentaire
- Hyperglycémie modifie la flore
- Collagène altéré par l'hyperglycémie chronique
- Altération de la vascularisation gingivale
- Prise en charge :
- Contrôle du diabète
- Hygiène buccale : brossage pluriquotidien, fil dentaire, produits de rinçage luttant contre la plaque dentaire
- Soins dentaires de prévention primaire et secondaire, consultation tous les 6 mois
Complications métaboliques
Coma céto-acidosique
- Définition du coma céto-acidosique :
- Acétonurie ≥ 2 +
- Glycosurie > 2 +
- Glycémie ≥ 2,5 g/L
- pH veineux < 7,25
- Bicarbonate < 15 mEq/L
Etiologie
- Déficit absolu en insuline inaugural (DT1) ou arrêt d'insulinothérapie
- Déficit relatif en insuline : diabète (pas forcément insulinodépendant) + facteur surajouté : IDM, infection, corticothérapie...
- Cause inconnue : 25%
Diagnostic
- Phase de cétose : syndrome cardinal aggravé + troubles digestifs (N/V, douleurs abdominales)
- Phase de céto-acidose :
- Dyspnée de Kusmall, troubles de la conscience, déshydratation mixte
- Diagnostic par BU + gaz du sang
- Ionogramme en urgence pour la kaliémie
- Critères de gravité :
- Sujet âgé
- pH < 7
- Kaliémie < 4 ou > 6
- Coma profond
- Instabilité tensionnelle
- Non-reprise de diurèse après 3h
- Vomissements incoercibles
- Diagnostic différentiel : urgence abdominale, coma hyperosmolaire (natrémie corrigée ++)
- Evolution : régression sous traitement en 24-48h, risque de complications iatrogènes (œdème cérébral, surcharge hydrosodée)
Traitement
- Préventif : règles éducatives en cas de cétose → maintien des injections même si inappétence, acétonurie systématique si glycémie > 2,5 g/L
- Premiers gestes :
- Scope, surveillance biologique
- Si besoin : SNG, SV, bilan infectieux, bilan hépatique
- Traitement curatif :
- Insuline rapide IVSE à débit constant tant que dure la cétose
- Remplissage par SSI (4 à 7 L)
- Apports potassiques IVSE avec surveillance de la kaliémie
- G10 IV pour glycémie à 2,5 g/L
- Traitement du facteur déclenchant
Coma hyperosmolaire
- Décompensation du sujet âgé DT2, parfois inaugurale si polyurie compensée par boissons sucrées
- 30% de mortalité
- Cliniquement : déshydratation intense, troubles de la vigilance
- Diagnostic biologique :
- Glycémie > 6 g/L
- Osmolalité > 350 mOsm/kg
- Natrémie corrigée > 155 mEq/L : Na(mesuré) + 1,6 × (Glycémie(g/L)-1)
- Absence de cétose et d'acidose
- Facteurs de risque :
- Age > 80
- Infection aiguë
- Diurétiques
- Défaut d'accès aux boissons
- Corticothérapie
- Traitement :
- Mise en condition : VVP(C), prévention complications de décubitus
- Réhydratation prudente et lente selon le terrain, 6 à 10 L de SSI dans les 24h
- Insulinothérapie IVSE pour glycémie horaire > 2,5 g/L
- Surveillance : conscience, pouls, PA, température, diurèse, ionogramme, créatinine
- Traitement de l'affection causale
Hypoglycémies
- Inévitable chez les DT1 même bien équilibrés (3 à 5 hypoglycémies modérées/sem)
- Combattre les fausses croyances : pas mortelle, pas de séquelles cérébrales sauf si très prolongée
- Attention à l'alcoolisme concomitant
- Risque d'hypoglycémie sévère si non-perception ou perception tardive
- Causes fréquentes : repas sautés, effort physique non-pris en compte, erreur d'injection d'insuline
- Education +++